Садржај
Процентуална маса одређује проценат сваког елемента који формира хемијско једињење. Да бисте пронашли ову вредност, требаће вам моларна маса сложених елемената у грамима / моловима или број грама који се користи за стварање решења. Процентуална маса се може израчунати на једноставан начин помоћу основне формуле која дели масу елемента (или растворене супстанце) са масом једињења (или раствора).
Кораци
Метод 1 од 2: Проналажење процентуалне масе са датим масама
- Дефинисати једначину за проценат масе једињења. Основна формула једињења је: проценат масе = () к 100. Резултат морате помножити са 100 на крају да бисте вредности изразили у процентима.
- Маса хемијског једињења које вас занима је маса дата у задатку. Ако ова вредност није наведена, погледајте следећу Методу и научите како да пронађете процентуалну масу када маса није дата.
- Укупна маса једињења израчунава се додавањем маса свих елемената који се користе за стварање једињења или раствора.
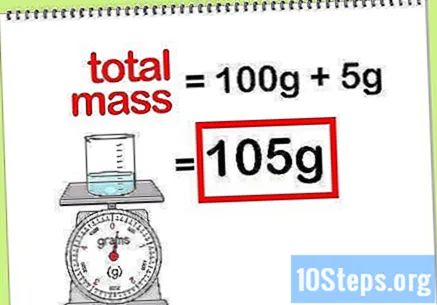
Израчунати укупну масу једињења. Када знате вредност масе свих доданих елемената или једињења, једноставно их требате збројити да бисте израчунали масу једињења или коначног раствора. Ова вредност ће бити називник у израчуну процентуалне масе.- На пример: Колики је проценат масе 5 г натријум хидроксида раствореног у 100 г воде?
- Укупна маса једињења је количина натријум-пероксида плус количина воде: 100 г + 5 г, укупне масе 105 г.

Утврдите масу хемикалије у питању. Када треба да пронађете проценат масе, проблем жели да пронађете масу одређеног елемента (предметни елемент) као проценат укупне масе свих елемената. Обратите пажњу на масу дотичног елемента. Ова вредност ће бити бројилац у израчуну процентуалне масе.- На пример, маса елемента је 5 г натријум хидроксида.
- Замените променљиве у формули процента масе. Након утврђивања вредности за сваку променљиву, замените их у једначини.
- На пример: проценат масе = () к 100 = () к 100.

Израчунајте проценат масе. Сада када је једначина формирана, само је решите да бисте израчунали проценат масе. Поделите масу елемента са укупном масом једињења и помножите са 100. Резултат ће бити процентуална маса хемијског елемента.- На пример: () к 100 = 0,04761 к 100 = 4,751%. Дакле, процентуална маса 5 г натријум хидроксида раствореног у 100 г воде је 4,751%.
Метод 2 од 2: Проналажење процентуалне масе са масама које нису дате
- Дефинисати једначину за проценат масе једињења. Основна формула за процентуалну масу једињења је: процентна маса = () к 100. Резултат морате помножити са 100 на крају да бисте вредности изразили у процентима.
- Када не знате вредности масе, можете да пронађете процентуалну масу елемента једињења помоћу моларне масе.
- На пример: Колики је проценат масе водоника у молекулу воде?.
Писати хемијска формула. Ако хемијске формуле за свако једињење нису дате, мораћете да их запишете. У супротном, пређите на корак „Пронађи масу сваког елемента“.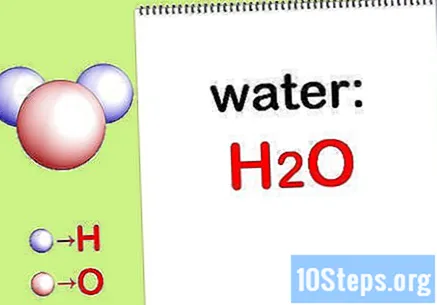
- На пример, напиши хемијску формулу за воду: Х.2ТХЕ.
Пронађите масу сваког елемента у једињењу. Потражите молекуларну тежину сваког елемента хемијских формула позивајући се на периодни систем. Генерално, маса елемента се може наћи испод симбола хемијског елемента. Обратите пажњу на масе сваког елемента једињења.
- На пример, молекулска маса кисеоника је 15,9994, а водоника 1,0079.
Помножите масе моларним односом. Утврдите колико мола има сваки елемент у хемијском једињењу. Број мадежа дат је претплаћеним бројем једињења. Помножите молекулску масу сваког елемента са моларним односом.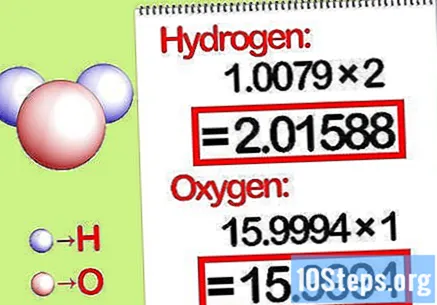
- На пример, моларни однос водоника према кисеонику у води је 2: 1. Према томе, помножите молекулску тежину водоника са два (1,00794 Кс 2 = 2,01588) и оставите молекуларну тежину кисеоника каква јесте (15,9994).
Израчунати укупну масу једињења. Сабрати укупну масу свих елемената једињења. Користећи масе израчунате моларним односом, могуће је израчунати укупну масу једињења. Овај број ће бити називник једначине процента масе.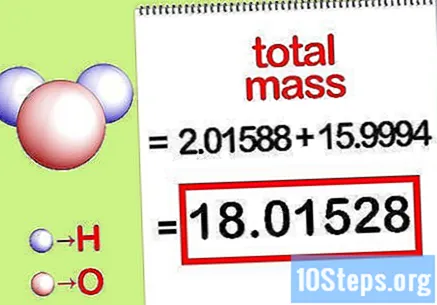
- На пример, додајте 2,01588 г / мол (маса два мола атома водоника) са 15,9994 г / мол (маса једног мола атома кисеоника) и добије се 18,01528 г / мол.
Идентификујте масу дотичног елемента. Када треба да пронађете проценат масе, проблем жели да пронађете масу одређеног елемента у једињењу као проценат укупне масе свих елемената. Утврдите масу дотичног елемента и запишите га. То је вредност масе израчуната помоћу моларног односа. Ова вредност је бројилац једначине процента масе.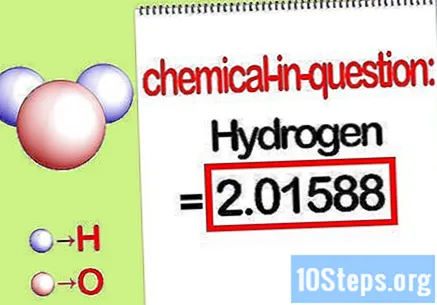
- На пример, маса водоника једињења је 2,01588 г / мол (маса два мола атома водоника).
- Замените променљиве у формули процента масе. Након одређивања вредности за сваку променљиву, замените их у једначини дефинисаној у првом кораку: процентна маса = () к 100.
- На пример: проценат масе = () к 100 = () к 100.
Израчунајте проценат масе. Сада када је једначина формирана, само је решите да бисте израчунали проценат масе. Поделите масу елемента са укупном масом једињења и помножите са 100. Резултат ће бити процентуална маса хемијског елемента.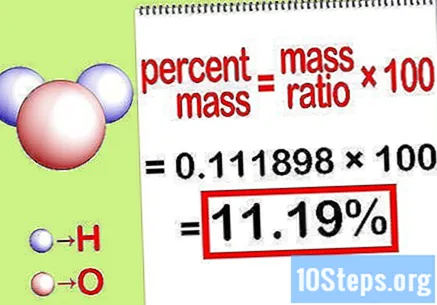
- На пример, проценат масе = () к 100 = 0,111189 к 100 = 11,18%. Дакле, процентуална маса атома водоника у молекулу воде износи 11,18%.