Садржај
Протони, неутрони и електрони су три главне честице које чине атом. Као што њихова имена сугеришу, први имају позитиван набој, други немају набој (неутрални су), а трећи негативни набој. Електрони имају врло малу масу, док протони и неутрони имају готово идентичну масу. Број сваког од њих у атому можете пронаћи користећи само информације из периодног система.
Кораци
Део 1 од 2: Израчунавање протона, електрона и неутрона
Набавите периодни систем. То је слика која организује елементе по атомској структури. Класификован је по бојама и даје сваком елементу јединствену скраћеницу од једног, два или три слова. Остале информације укључују атомску масу и број.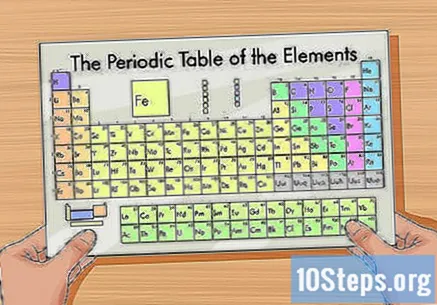
- Периодни систем можете пронаћи на мрежи или у књизи о хемији.
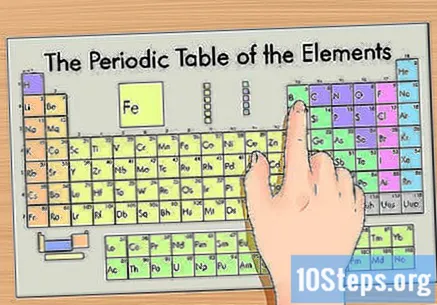
Пронађите свој елемент у периодном систему. Елементе организује према атомском броју и раздваја их у три главне групе: метале, неметале и металоиде (полуметали). Остале групе укључују алкалне метале, халогене и племените гасове.- Коришћење групе (колоне) или тачке (редови) може олакшати проналажење елемента у табели.
- Такође можете тражити симбол елемента ако не знате ниједну другу особину.
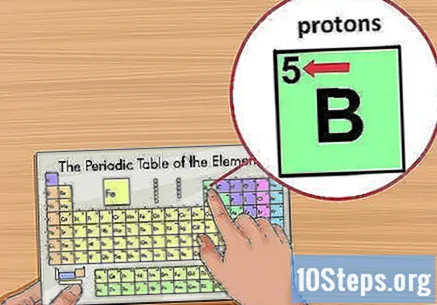
Пронађите атомски број. Налази се изнад симбола елемента, у горњем левом углу квадрата. Атомски број ће вам рећи колико протона формира један атом тог елемента.- На пример, бор (Б) има атомски број 5, а самим тим и пет протона.
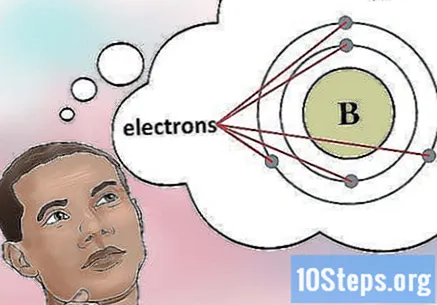
Одреди број електрона. Протони су честице у језгру атома које имају позитиван набој. Електрони су негативно наелектрисане честице. Стога ће неутрални елемент имати једнак број протона и електрона.- На пример, бор (Б) има атомски број 5, а самим тим и пет протона и пет електрона.
- Међутим, ако елемент укључује позитивни или негативни јон, протони и електрони неће бити исти. Мораћете да их израчунате. Јонски број ће се појавити као мали натпис након елемента.
Потражите атомску масу. Да бисте пронашли број неутрона, прво ћете морати да пронађете атомску масу. Ова вредност је просечна маса атома елемента и може се наћи испод симбола елемента.
- Заокружи атомску масу на следећи цео број. На пример, атомска маса бора је 10,811, али можете је заокружити на 11.
Одузми атомски број од атомске масе. Да бисте пронашли број неутрона, потребно је да од масе одузмете атомски број. Запамтите да је атомски број једнак броју протона, који је већ идентификован.
- За наш пример за бор, 11 (атомска маса) - 5 (атомски број) = 6 неутрона
Део 2 од 2: Израчунавање електрона са присутним јонима
Утврдите број јона. Појавиће се као мала натписна вредност након елемента. Јон је атом са позитивним или негативним наелектрисањем због додавања или уклањања електрона. У јону, иако број протона остаје исти, број електрона се мења.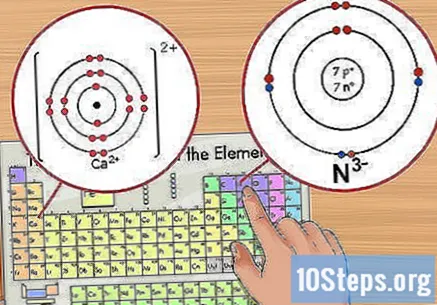
- Пошто електрон има негативан набој, када се уклони, јон постаје позитиван. Како се додаје више електрона, јон постаје негативан.
- На пример, Н има наелектрисање -3, док Ца има наелектрисање +2.
- Имајте на уму да овај прорачун не треба да радите ако иза елемента не постоји надређени број.
Одузми наелектрисање од атомског броја. Када јон има позитиван набој, атом је изгубио електроне. Да бисте израчунали преосталу количину њих, од атомског броја одузмите износ додатног наелектрисања. У случају позитивног јона, има више протона него електрона.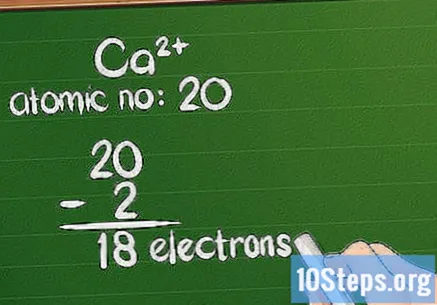
- На пример, Ца има +2 наелектрисање, па је изгубио 2 електрона из свог природног стања. Атомски број калцијума је 20, тако да јон има 18 електрона.
Додајте наелектрисање атомском броју негативних јона. Када јон има негативан набој, атом је стекао електроне. Да бисте израчунали укупан број њих, атомском броју само додајте количину додатног наелектрисања. У случају негативног јона, има мање протона него електрона.
- На пример, Н има наелектрисање -3, па је добио три електрона у поређењу са својим неутралним стањем. Атомски број азота је 7, тако да овај јон има 10 електрона.